检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
2017年4月10日,哈佛大学医学院、Dana-Farber癌症研究所Piotr Sicinski教授研究组与beat365官方网站、北大-清华生命科学联合中心、统计科学中心李程研究组合作,在《Cancer Cell》期刊发表了题为 “Cell-Cycle-Targeting MicroRNAs as Therapeutic Tools against Refractory Cancers”的论文。
细胞的分裂与增殖是由细胞周期蛋白(cyclin)及依赖它们的激酶(CDK)驱动和控制的。对人类癌症样本的分析显示,细胞周期蛋白和CDK的过表达是癌症发病机制中的重要因素。然而靶向细胞周期机制的临床药物研究至今受到限制,原因可能是多个细胞周期蛋白和CDK的互相补偿机制。先前的研究发现部分微小RNA(miRNA)能够靶向细胞周期蛋白和CDK,但没有研究系统地描述这类miRNA。在本项研究中,Sicinski研究组提出假说,通过miRNA抑制多种细胞周期蛋白和CDK的表达水平可以选择性地阻断癌细胞的增殖,并且减少细胞周期补偿机制的发生。
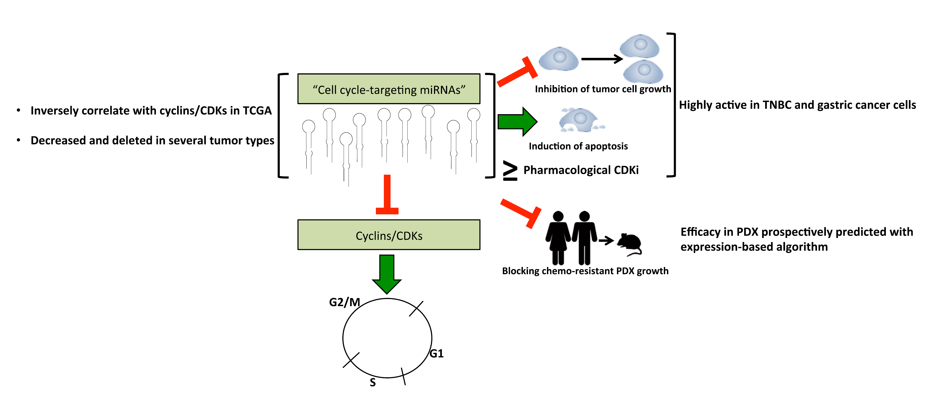
图片来源:《Cancer Cell》同期评述
“Not So Fast: Cultivating miRs as Kinks in the Chain of the Cell Cycle”by Schiewer and Knudsen.
在本项研究中,Sicinski研究组首先实验筛选调节细胞周期蛋白的miRNA。对于表达荧光素酶基因与一种细胞周期蛋白或CDK的3’UTR的融合基因的细胞系,分别转染885个人类miRNA。靶向某个细胞周期蛋白或CDK的3’UTR的miRNA的表达将会抑制相应荧光素酶的表达。实验筛选后发现了部分miRNA能够靶向多个细胞周期蛋白和CDK。李程研究组继而利用生物信息学方法进一步筛选这些候选miRNA,包括miRNA靶基因的预测、靶基因的通路富集、TCGA数据中基因表达和miRNA表达的负相关性等方法。筛选结果得到miR-195, miR-193a, miR-214 等miRNA为调控细胞周期通路的重要因素。
Sicinski研究组随后利用包括多个癌症类型的CCLE细胞系验证它们对这些miRNA过表达的反应,证明了这些miRNA对不同癌症细胞类型具有抑制增殖、促进凋亡的效果,并发现miR-193a-3p对于最难以治疗的乳腺癌类型之一——三阴乳腺癌的细胞抑制作用最为明显。利用纳米颗粒的形式递送miR-193a-3p,能够抑制七种小鼠异种移植模型中的肿瘤生长,包括三种复发性癌症患者来源的肿瘤。这些研究结果证明了应用靶向细胞周期的miRNA可以抑制难以治疗的癌症类型,并且对比实验证明应用这些miRNA的效果优于目前可用的治疗药物。另外,通过将人类癌细胞系的基因表达谱与它们对单个miRNA过表达的反应相关联,李程研究组开发了基于弹性回归网络的算法,可以预测特定原发肿瘤对给定miRNA药物的反应。这些结果为基于基因组学的个体化癌症治疗提供了实验依据。
该研究得到北大-清华生命科学联合中心、科技部国家重点研发计划、国家自然科学基金的资助。Piotr Sicinski教授和李程研究员是该论文的通讯作者,北京大学生命科学中心13级博士生王轶楠、10级本科生金冲、清华大学生科院13级本科生李晓婷、同济大学生科院12级博士生李鹰翔对本项研究做出了重要贡献。
论文链接:http:// www.cell.com/cancer-cell/fulltext/S1535-6108(17)30100-9
Sicinski教授发表的相关综述:Nat Rev Cancer. 2017. Cell cycle proteins as promising targets in cancer therapy.https://www.ncbi.nlm.nih.gov/pubmed/28127048
北京大学生科院生物信息平台论坛:http://forum.cbi.pku.edu.cn/(公众号:wegenome)